阿爾茨海默病(Alzheimer's disease, AD)是主要的癡呆類型之一。其主要的病理特征是β澱粉樣蛋白形成的斑塊和過度磷酸化tau蛋白形成的神經纖維纏結,并伴有突觸功能障礙和神經炎症反應。在臨床上,AD最重要的表現是進行性認知能力下降。在大腦中,神經元和膠質細胞之間的細胞通訊在協調大腦生理功能方面起着關鍵作用。然而,神經元中病理性tau是否會幹擾星形膠質細胞,調控AD的疾病發生仍不清楚。
最近,一些研究揭示了腺苷及其受體在各種神經系統疾病的神經調節和神經保護作用中的關鍵作用。已知存在4個腺苷受體,分别是A1、A2A、A2B和A3。腺苷受體A1(A1R)是一種抑制性腺苷受體,在大腦中表達量較高。給予咖啡因(一種非選擇性A1R拮抗劑),可以減輕Aβ病變,對AD有保護作用。此外,敲除A1R可以改善老年小鼠的炎症反應[11]。但A1R在介導AD認知障礙和突觸損傷的作用機制仍不明确。
2023年4月21日,華中科技大學朱鈴強教授團隊在Science Advances上發表題目為Tau pathology epigenetically remodels the neuron-glial cross-talk in Alzheimer's disease 的文章,發現了病理性Tau蛋白通過影響神經元A1R/Lcn2通路,調控神經元-星形膠質細胞的Cross-talk,參與AD認知障礙和突觸損傷,為AD治療提供了新靶點。

朱鈴強團隊的研究證實,A1R蛋白在AD患者、AD病人來源的iPSC、3×Tg和P301L-AD模型小鼠中上調表達,并且A1R蛋白表達水平與磷酸化的Tau蛋白具有正相關性。但其mRNA表達在AD中并無變化,經過動物體内和細胞體外的實驗研究,發現磷酸化Tau可以通過Mef2c/miR-133a-3p,在轉錄後水平表觀遺傳調控A1R的表達。
在野生型C57小鼠的海馬神經元中特異性過表達A1R後,小鼠出現學習記憶障礙和突觸損傷,并發現星形膠質細胞過度活化和炎症因子的高量表達;此外,在3×Tg小鼠海馬神經元特異性幹擾A1R後,可以緩解其記憶障礙和突觸損傷,過度活化的星形膠質細胞被抑制,炎症因子的表達量也明顯降低,同時Aβ生成和Tau磷酸化水平也都明顯降低。
随後原代細胞實驗發現,用過表達A1R的原代神經元的培養基,處理原代星形膠質細胞,導緻其過度活化。利用iPSC技術,用AD病人iPSC神經元培養基預處理的星膠,再用此星膠和神經元共培養,結果發現,與對照iPSC神經元培養基預處理的星膠相比,AD病人iPSC神經元培養基預處理的星膠能明顯降低神經元sEPSCs幅度。
進一步通過轉錄組測序發現,A1R敲除小鼠海馬中,脂質運載蛋白2(Lipocalin-2, Lcn2)表達顯著降低,并發現Lcn2在3×Tg小鼠上調,且在過表達A1R的原代神經元培培養基中含量增加。進一步敲除3×Tg小鼠中A1R,發現AD中過度活化的星形膠質細胞被抑制,Lcn2和炎症因子的表達都降低,認知障礙和突觸損傷得到緩解。
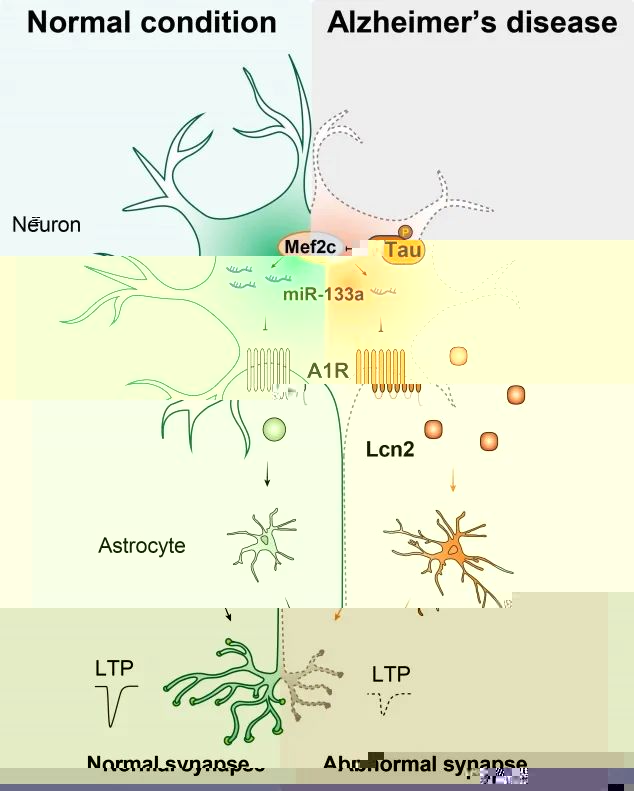
圖1 工作機制圖
綜上,在AD神經元中病理性tau蛋白表觀遺傳學調控A1R的表達,導緻神經元表達和分泌Lcn2明顯增加,從而激活星形膠質細胞,誘發AD神經炎症反應,最終導緻突觸損傷和認知功能障礙(圖1)。
華中科技大學88858cc永利官网病理生理學系2017級博士研究生周蘭庭、醫學遺傳學系劉丹教授和附屬同濟醫院神經内科康慧聰主任為該論文的共同第一作者,朱鈴強教授和魯友明教授為論文的共同通訊作者。
論文鍊接:http://doi.org/10.1126/sciadv.abq7105
 學院官方微信
學院官方微信